<目次>
1. まえがき
2. 化学反応の自由エネルギー変化ΔG
3. 標準自由エネルギー変化ΔG0の計算の仕方
4. ケーススタディ
4.1 たたら製鉄~酸化鉄の炭素による還元反応
4.2 水素製鉄~酸化鉄の水素による還元反応
5. あとがき
1. まえがき
物質と物質との間の化学反応が起こりうるかどうかを知ることは、化学反応を伴う物質・材料の生産を適切・効率よく行うために重要である。また、その際に有害物質が発生するかどうかを知ることは安全上も重要な問題である。化学反応の起こりやすさを判断する指標としては、反応前後の自由エネルギーの変化ΔGがある。すなわち、反応前後の自由エネルギーGが減少する方向(ΔG<0)に反応は進み、自由エネルギーGが増加する方向(ΔG>0)には反応が起こらない。ここでは、化学反応が起こる方向を示す自由エネルギー変化ΔGの求め方について解説し、いくつかのケーススタディについて紹介したい。
2. 化学反応の自由エネルギー変化ΔG
自由エネルギーGとは系の内部エネルギーのうち仕事として取り出せるエネルギーであり、エンタルピーHとエントロピーSという熱力学量と絶対温度Tを用いると[1]式のように表せる。
G=H-TS・・・[1]
詳細は略すが、構成分子の乱雑さを表すエントロピーSは比熱CPを用いて絶対値を求めることができる。一方、反応熱に相当するエンタルピーHはエントロピーSと同様に比熱CPと関連付けられる熱力学量であるが、絶対値を求めることはできない。したがって、[1]式よりわかるように、自由エネルギーGの絶対値は求めることはできない。ただし、幸運にも、反応熱を基に反応前後のエンタピー変化ΔH求めることができるので,自由エネルギーの変化ΔGも求めることができることとなる。
ΔG=ΔH-TΔS・・・[2]
ここで、物質Aと物質Bを反応させて新しい物質Cと物質Dを製造する[3]式で示す化学反応を考えてみる。
A+B=C+D・・・[3]
物質A、B、C、Dが持つ自由エネルギーGを各々GA、GB、GC、GDとすると、[3]式の反応の自由エネルギー変化ΔGは次のように表される。
ΔG=(GC+GD)-(GA+GB)・・・[4]
各々の物質の自由エネルギーGA、GB、GC、GDは先に述べたように、残念ながら絶対値は不明である。ただし、標準状態(25℃、1気圧)で最も安定な元素の単体を基準(自由エネルギーゼロ)として、そこから1モルの物質が生成する際の自由エネルギー変化で定義される標準生成自由エネルギーΔfGoは求めることができ、この値は各種のデータベースに収録されている。この標準生成自由エネルギーΔfGoを用いて、[4]式は[5]式のように書き直せる。
ΔfGo={ΔfGo(C)+ΔfGo(D)}-{ΔfGo(A)+ΔfGo(B)}・・・[5]
3. 標準自由エネルギー変化ΔGoの計算の仕方
ここでは、JANAF(注)から公表されている熱化学データベースを用いて、ケーススタディを行う。化学反応としては、まず、[6]式の炭素Cと酸素O2との燃焼反応を考えてみる。
C(s)+O2(g)=CO2(g) ・・・[6]
各々の反応成分の標準生成自由エネルギー変化ΔfGoをΔfGo(C)、ΔfGo(O2)、ΔfGo(CO2)とすると、[6]式の化学反応の標準自由エネルギー変化ΔGoは、[5]式にしたがって[7]式のように書ける。
ΔGo=ΔfGo(CO2)-{ΔfGo(C)+ΔfGo (O2)}・・・[7]
表1に示す298K(25℃)のデータで計算すると、
ΔGo[298K]=-394.389-{0+0}=-394.389 kJ/mol・・・[8]
[6]式の化学反応の標準自由エネルギー変化ΔGoは、-394.389 kJ/mol でマイナスであるので炭素Cと酸素O2との燃焼反応は25℃で起こりうるということになる。 バーべキューの木炭が勝手に燃えてしまうということになるのだが、実際は化学反応が起こる状態まで活性化させるエネルギー(活性化エネルギー)が必要であり、そう簡単にはいかないことに注意が必要である。図1に自由エネルギー変化と活性化エネルギーの概念図を示す。化学熱力学で予測できるのは、あくまで反応が起こりうるということである.いわゆる、反応が起こるための必要条件ということである。
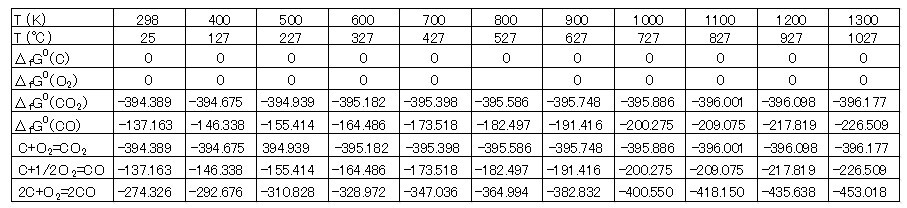
表1 C, O2, CO2, CO の標準生成自由エネルギー変化ΔfGo [JANAF]
さらに、「α、β」等のギリシャ文字に対応した点字コードデータも準備した。そのデータの一部を図13に示す。
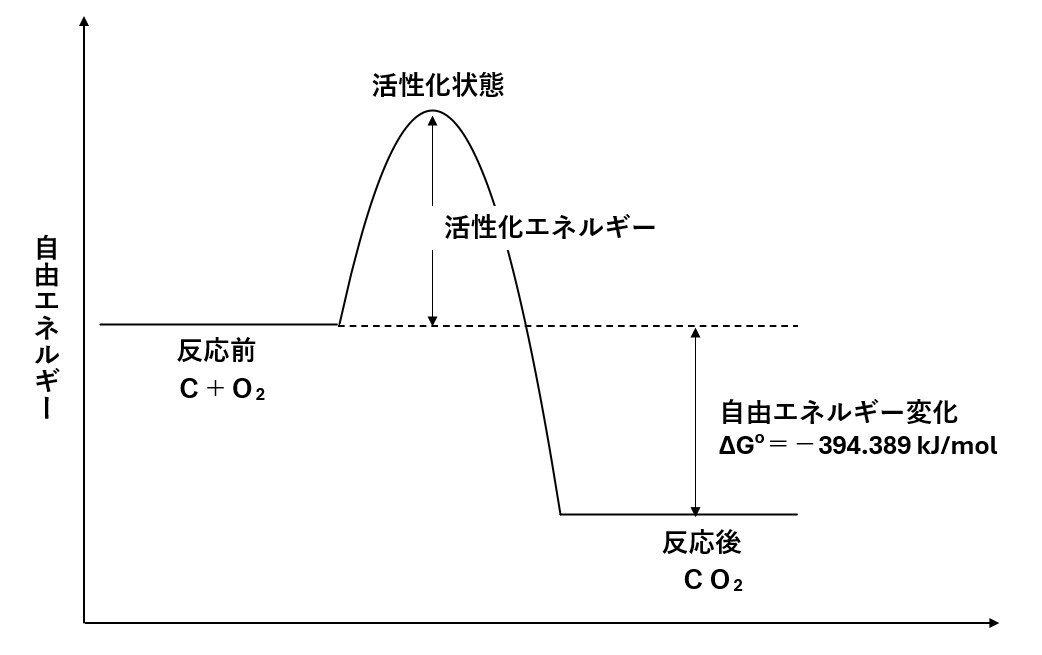
図1 自由エネルギー変化と活性化エネルギーの概念図
つぎに、炭素Cと酸素O2との燃焼反応として、[9]式で表されるCOガスが生成する不完全燃焼反応を考えてみる。
C (s)+1/2O2(g)=CO(g)・・・[9]
表1に示した298K~1300Kの範囲での標準自由エネルギー変化ΔGoの計算結果からは、ΔGo[CO2]<ΔGo[CO]で一見COの生成反応は優先して起こらないように見える。しかし、[10]式に示す酸素O2 1molの消費反応と置き換えると、
2C(s)+O2(g)=2CO(g)・・・[10]
図2に[6]式のCO2生成反応と[10]式の2COの生成反応の標準自由エネルギー変化ΔGoの計算結果を示す。酸素O2 1mol当たりで比較すると、1000K以上の高温域では、ΔGo[CO2]>ΔGo[CO]と逆転しCOの生成反応が優先して起こりうるようになる。すなわち,炭素Cと酸素O2との燃焼反応では、低温域ではCO2(還元能力がないガス)の生成、高温域ではCO(還元能力があるガス)の生成が優先的に起こることを意味している。
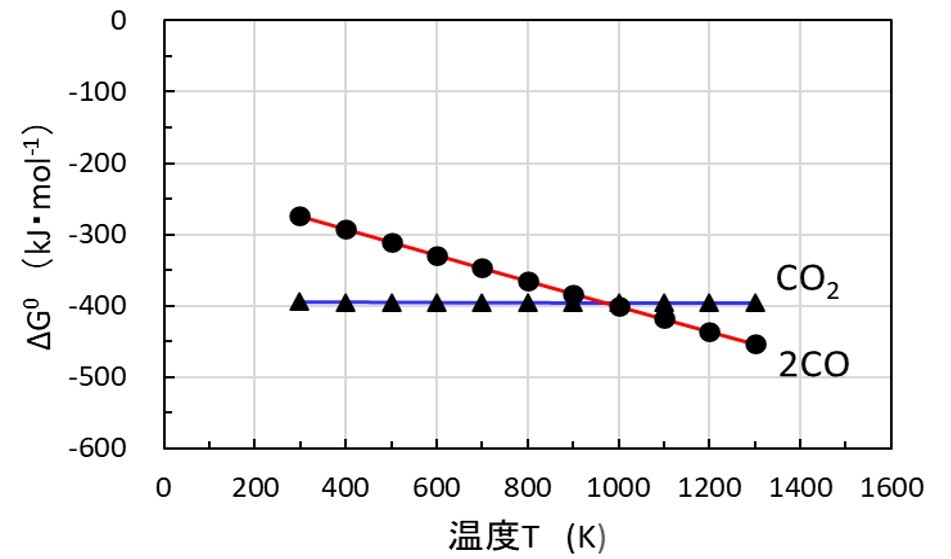
図2 CO2と2COの生成反応の標準自由エネルギー変化
化学熱力学では化学反応式の加減則が適用できるので,[10]式-[6]式の操作を行うと、
C(s)+CO2(g)=2CO(g)・・・[11]
この反応はブードア反応(Boudouard reacton)と呼ばれ、製鉄業では高炉内のガス反応において重要な役割をはたす。また、炭素と酸素の反応が伴う化学工業や冶金プロセスでも重要な反応である。図3は[11]式の化学平衡における生成ガス中のCOガスの分圧(PCO/PCO+PCO2)を計算した結果である。炭素Cが共存する高炉内のような条件では、600K以下の低温域ではCO2ガスの生成が支配的で、1300K以上の高温域ではCOガスの生成が支配的であることがわかる.ここでは詳細な導出は省略する。
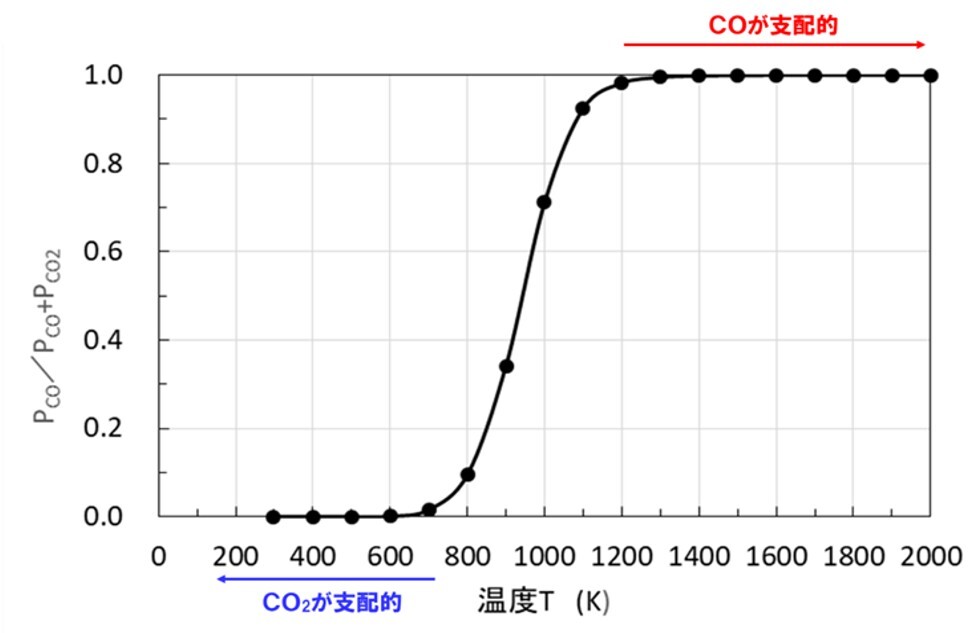
図3 C共存下でのCO2とCOのガス割合
(注)JANAFについて
JANAFとは、
Joint Army-Navy-Air Forceの略で、陸軍-海軍-空軍の合同の頭文字をとったものである。1950年代米国でロケット燃料に関する熱力学データベースを確立するプロジェクトが、米国国防総省(U.S.
Department of Defense)がスポンサーとなってダウ・ケミカル(The
Dow Chemical Company)によって行われた。この熱力学データベースは化学ロケットの推進はもとより様々な技術分野で利用されるようになり、米国商務省(U.S.
States Department of Commerce)配下の国立標準局NBS(National
Bureau of Standards)の標準参考データシステム(National
Standard Reference Data System)に編入され1971年に公開された。1988年にはNBSは改組され、国立標準技術研究所NIST(National
Institute of Standards and Technology)に引継がれ現在に至っている。1998年NIST-JANAF
Thermochemical Tables 4th ed.1)が刊行され,インターネット上でも公開(フリーアクセス可)されている。
1)
NIST-JANAF Thermochemical Tables 4th ed. (Journal of Physical and
Chemical Reference Data, Monograph No.9), Malcolm W. Chase, Jr (ed.), American Institute of
Physics, (1998).
(https://janaf.nist.gov/: NIST-JANAF Thermochemical Tables, 2026年2月公開中)
4. ケーススタディ
4.1 たたら製鉄~酸化鉄の炭素による還元反応
たたら製鉄は砂鉄と木炭を主原料とする日本古来の製鉄法である.また、近年では比較的小規模で操業できることから、原料から製品造りまで一貫で体験できるものづくり教育の素材として注目されている。北九州市が実施していた「東田たたらプロジェクト」は小学生を対象とし、大学生や社会人も加わり非常に人気が高かった。
たたら製鉄での基本反応は、砂鉄Fe3O4の木炭Cによる還元反応であり,図4にたたら製鉄と高炉製鉄の比較を示すように、鉄鉱石Fe2O3のコークスCによる還元反応である高炉内の化学反応とほぼ同じである。また、酸化鉄スケールや酸化鉄スラッジなどの廃棄物から炭素Cを利用して鉄分を回収しようとする際に参考となる基本的な反応でもある.
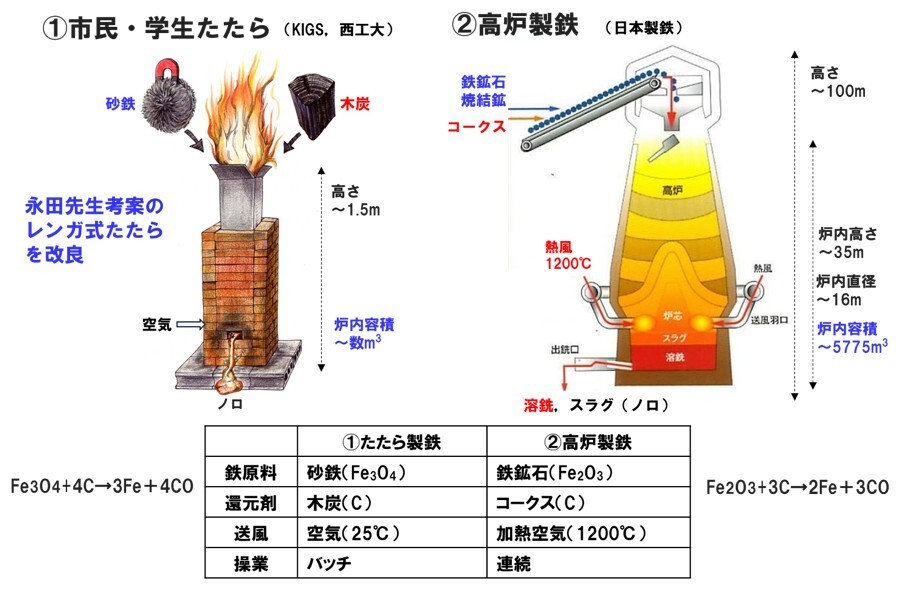
図4 レンガ式たたら製鉄と高炉製鉄の比較
たたら製鉄炉内の還元反応としては、上述したように炭素Cが共存する条件では、低温域ではCO2ガスの生成が支配的であること、および、高温域ではCOガスの生成が支配的であることを考慮すると、次のような反応式を想定することができる。
Fe3O4(s)+2C(s)=3Fe(s)+2CO2(g)・・・[12]
Fe3O4(s)+4C(s)=3Fe(s)+4CO(g)・・・[13]
[12]式と[13]式の反応の標準自由エネルギー変化ΔGo は各々[14]式と[15]式のように表される。
ΔGo[12]={3ΔfGo(Fe)+2ΔfGo(
CO2)}-{ΔfGo(Fe3O4)+Δ2fGo
(C)}・・・[14]
ΔGo[13]={3ΔfGo(Fe)+4ΔfGo(
CO)}-{ΔfGo(Fe3O4)+4ΔfGo (CO)}・・・[15]
表2に各々の反応成分の標準生成自由エネルギー変化fGoの値、および、各反応式の標準自由エネルギー変化
ΔGoの計算結果(298K~1700K)を示す. Fe3O4(s)のC(s)による還元反応は約1000K(727℃)以上で起こりうることがわかる。また、CO(g)が生成する[13]式の反応の標準自由エネルギー変化ΔGoの方が負の大きな値であり起こりやすいと考えられる。したがって、たたら製鉄のような酸化鉄Fe3O4(砂鉄)を炭素C(木炭)で還元するプロセスでは反応炉内を約1000K(727℃)以上に加熱することが重要であると言える。
一方、[13]式の反応で生成したCOガスは還元応力を有したガスであるので、次の還元反応も考えることができる。
Fe3O4(s)+4CO(s)=3Fe(s)+4CO2(g)・・・[16]
Fe3O4(s)+CO(s)=3FeO(s)+CO2 (g)・・・[17]
FeO(s)+CO(s)=Fe(s)+CO2
(g)・・・[18]
表2に示した各反応式の標準自由エネルギー変化ΔGoの計算結果を見ると、[17]式で示した還元反応は広い温度範囲で起こりうることがわかる。このような生成したCOガスによる還元反応を間接還元反応と言い、固体炭素Cによる還元反応を直接還元反応と言う。通常、還元剤であるCOガスの反応界面での物質移動が速い間接還元の方が、還元剤である固体Cの反応界面での物質移動が遅い直接還元よりも支配的であるとされている。
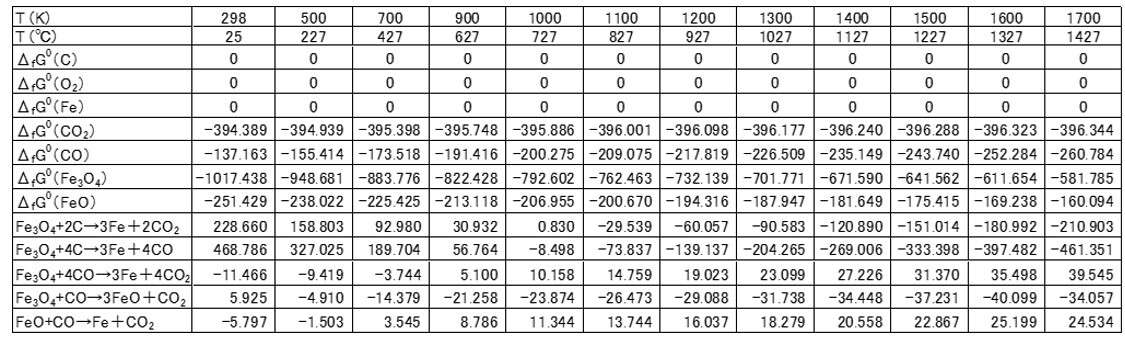
表2 酸化鉄のC還元に関する各反応成分の 標準生成自由エネルギー変化ΔfGo [JANAF]
4.2 水素製鉄~酸化鉄の水素による還元反応
環境問題としてCO2の排出削減が課題となっており、その対策の一つとして酸化鉄の還元剤として還元性のH2ガスの適用が検討されている。図5に炭素還元製鉄と水素還元製鉄の概念図を示す.鉄鉱石Fe2O3の水素H2による還元反応は、[19]式のように表されるが,高炉内では上部から下部に向かってFe2O3→Fe3O4→FeO→Feの順で還元されていると考えられることが多く,各々の素反応は[20]式~[22]式のように表される。[19]式の反応式は総括反応式と言える。いずれの反応式でも反応生成物としてCO2ガスは生成されず、H2Oガスが生成されるので、クリーンな製鉄法と言われるわけである。
Fe2O3(s)+3H2(g)=2Fe(s)+3H2O(g)・・・[19]
3Fe2O3(s)+H2(g)=2Fe3O4(s))+H2O(g)・・・[20]
Fe3O4(s)+ H2(g)=3FeO(s)+H2O(g)・・・[21]
FeO(s)+H2(g)=Fe(s)+H2O(g)・・・[22]
表3に各々の反応成分の標準生成自由エネルギー変化ΔfGoの値、および、各反応式の標準自由エネルギー変化ΔGoの計算結果(298K~1700K)を示す。また、図6には各反応式の標準自由エネルギー変化ΔGo温度依存性をグラフ化した。これらの図表からわかることは,約1000K以上の高温状態とすることで、酸化鉄の水素還元が起こりうることがわかる。ただし、注意しないといけないことは酸化鉄の炭素C還元反応は総括的には発熱反応であるため外部からの熱の供給は不要と考えてもいいが、水素H2還元反応は総括的には吸熱反応であるため外部からの熱供給が必要となる。結果的に、熱供給が不十分な場合は固体鉄、半溶融鉄の生産となるため、電気炉との組合せ等が必要となる.
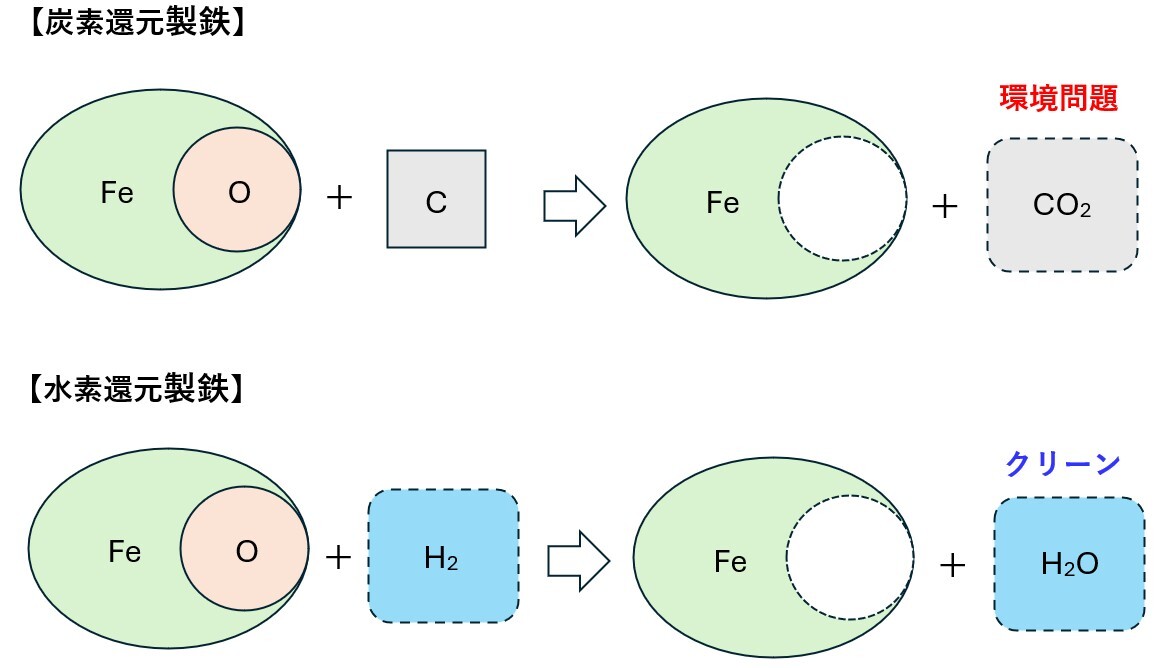
図5 炭素還元製鉄と水素還元製鉄の概念図
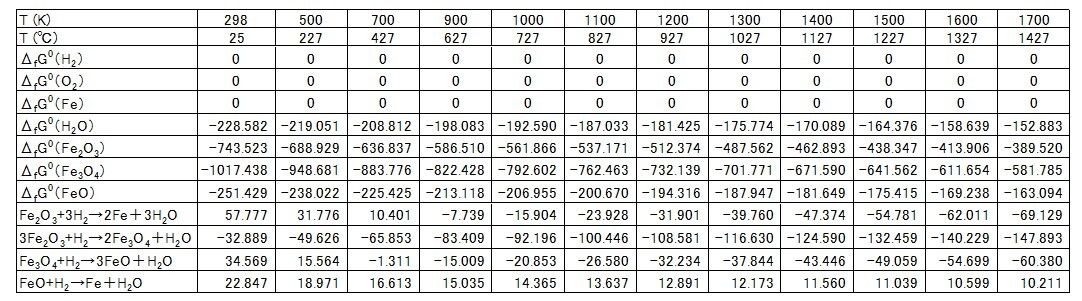
表3 酸化鉄のH2還元に関する各反応成分の 標準生成自由エネルギー変化ΔfGo [JANAF]
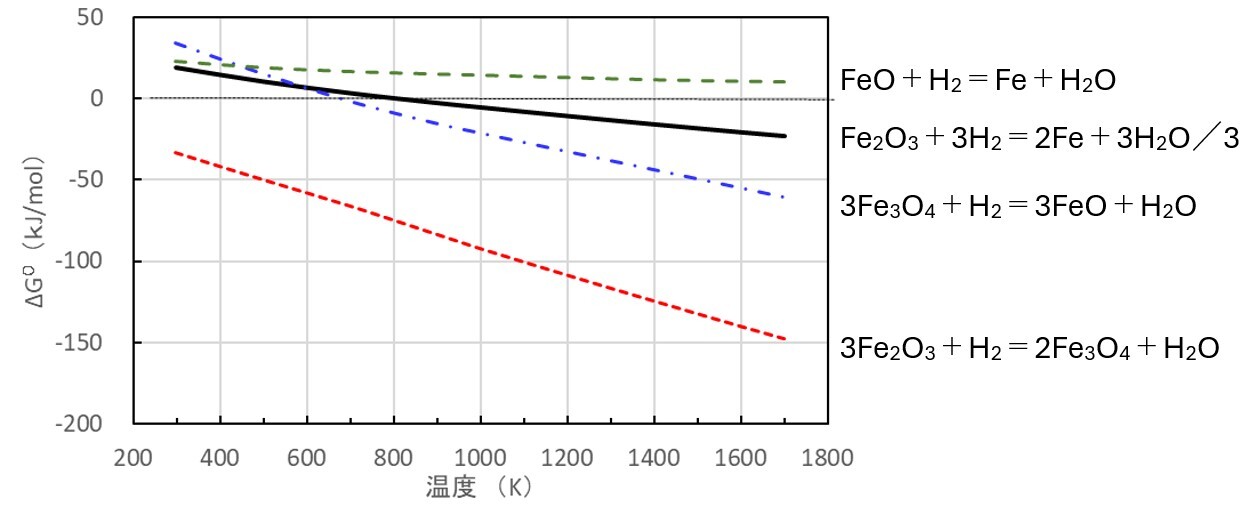
図6 酸化鉄の水素還元反応の標準自由エネルギ変化
つぎに、耐火物と水素H2の反応について、耐火物成分としてよく使われるSiO2、Al2O3との反応を考えてみる。1700K、1気圧のような高温では、不安定ガスであるSiO(g)、Al2O(g)の生成も考慮すると、つぎのように標準自由エネルギー変化ΔGoを計算できる。
SiO2(s)+2H2(g)=Si(L)+2H2O(g)・・・[23]
ΔGo={ΔfGo(Si)+2ΔfGo(H2O)}-{ΔfGo(SiO2)+2ΔfGo
(H2)}
={0+2×(-152.883)}-{-609.059+2×0}=303.293 kJ/mol
SiO2(s)+H2(g)=SiO(g)+H2O(g) ・・・[24]
ΔGo={ΔfGo(SiO)+ΔfGo(H2O)}-{ΔfGo(SiO2)+ΔfGo (H2)}
={(-242.737)+(-152.883)}-{-609.059+0}=213.439 kJ/mol
Al2O3(s)+3H2(g)=2Al(L) +3H2O(g)・・・[25]
ΔGo={2ΔfGo(Al)+3×ΔfGo(H2O)}-{ΔfGo(Al2O3)+3ΔfGo
(H2)}
={2×0+3×(-152.883)}-{-1131.342+3×0}=825.576 kJ/mol
Al2O3(s)+2H2(g)=Al2O(g) +2H2O(g)・・・[26]
ΔGo={ΔfGo(Al2O)+2×ΔfGo(H2O)}-{ΔfGo(Al2O3)+2×ΔfGo
(H2)}
={(-263.368)+2×(-152.883)}-{-1131.342+2×0}=562.208 kJ/mol
これらの計算結果からわかるように、いずれの反応もΔGo>0であり、SiO2やAl2O3の耐火物成分自体は1700KではH2によって簡単には還元されないことがわかる.ただし、圧力が変化した減圧条件等では状況は変わることもあるので注意が必要である。
【JANAFの熱力学データの入手手順】
一例として,Cについて、NISTのホームページからの入手手順について以下に説明する。
手順① インターネットプラウザの検索画面で『JANAF』で検索する。
手順② 『NIST-JANAF Thermochemical
Tables』が出てくるのでクリックする。
手順③ NIST-JANAF Thermochemical
Tables画面内の『周期律表』をクリックする。
手順④ 周期律表が拡大表示されるので、炭素『C』をクリックする。
手順⑤ 炭素Cを含む物質のリストがアルファベット順で出てくるので、『C Carbon ref』の
『view』をクリックする。
手順⑥ 温度Tが0Kから6000Kまで、100K毎に、比熱Cp0、エントロピーS0、生成エンタルピーΔfH0、
標準生成自由エネルギーΔfG0、平衡定数logKfなどの値が掲載されている表が表示される。
手順⑦ この表から例えば1000KでのCの標準生成自由エネルギーとして、ΔfG0=0
kJ・mol-1を得る。
単位からわかるように、物質(ここではC)1mol当りのエネルギーとして表されいる。
なお、JANAFの熱力学データベースでは、元素の標準状態(Reference State)は『ref』と表示されており、元素または単体の標準状態での生成自由エネルギーΔfG0は、約束により、ΔfG0=0である。また、圧力はP=0.1MPaを標準状態とした値が掲載されているが、P=1atm=0.1013MPaでもほぼ問題なく使えると考えてよい。
注意: データベース自体は2026年2月現在インターネット上で無料公開されているが、引用する場合は出典を明示すること。
例)
NIST-JANAF Thermochemical Tables 4th ed. (Journal of Physical and
Chemical Reference Data, Monograph No.9), Malcolm W. Chase, Jr (ed.), American Institute of
Physics, (1998).
(https://janaf.nist.gov/:
NIST-JANAF Thermochemical Tables, 2026年2月公開中)
5. あとがき
私は、製鉄メーカーを退職後、縁あって耐火物メーカ―や耐火物の研究機関で化学熱力学の講師をやることになりました。大学で材料・化学系出身者で化学熱力学について講義を受け、自由エネルギー変化ΔG等の知識を学んだ人は多かったと思います。ただし、実践で使う機会が少なく、いざ計算となると苦労されてるように思いました。化学熱力学自体はすでにほぼ完成された学問で、現在では計算機の能力向上により条件を入力するだけで自由エネルギーΔGの計算だけでなく、反応が起こった後の状態(平衡状態)まで予測できるようになっています。計算熱力学と言われるもので、数種の計算ソフトが公開され、上手に使いこなすとプロセスの適切な制御だけでなく新しい技術の開発にもつながる貴重なツールになるものです。そのためにはブラックボックス的でなく計算の中身をよく理解することが必要であると思います。まずは基礎的な自由エネルギー変化ΔGの計算の仕方をマスターし応用・発展させていくことで、製造現場での課題の解決だけでなく新技術開発の一助になれば幸甚に思います。
本記事の内容については、ご利用者様自身の判断と責任において、ご活用頂くようお願いいたします。日本技術士会が本記事の正確性や有用性等を保証するものではありません。

【執筆者】
ZEZE技術士事務所
代表 瀬々 昌文
技術士(金属)
(日本技術士会九州本部/北九州)
【専門事項】
製鉄メーカーで32年間製鋼プロセスの研究開発、とくに連続鋳造プロセスの新技術開発・技術改善、連続鋳造鋳片の品質対策に従事
退職後9年間工業大学の機械工学科教授として,機械材料・材料力学・非破壊検査技術、工業英語等の講義を担当しながら、たたら製鉄によるものづくり人材教育を支援・協力
技術士一次試験(機械・金属)の受験指導(8年間で37名の合格者輩出)
機械設計技術者三級、第三種電気主任技術者、第一級陸上特殊無線技士、第一級アマチュア無線技士、
甲種危険物取扱者、エックス線作業主任者
※本記事のご利用にあたって
本記事の内容は執筆者個人の見解に基づくものであり、日本技術士会の公式見解ではありません。また、記事の内容は執筆時点の情報に基づいています。ご利用者様自身の判断と責任において、ご活用頂くようお願いいたします。











