<目次>
1. はじめに
2. 溶射とは (溶射技術のイロハ)
3. 鉄鋼材料はなぜ錆びる?
4. 防食溶射技術の紹介
5. おわりに
1. はじめに
2025年10月現在,鋼材の種類にもよるが鋼材の凡その価格は,1トンあたり12〜13万円で推移している.1kgあたり約130円となり,市販のミネラルウォーター(約200円/L(1kg))より安いことになる.鉄鋼材料は他の金属材料より圧倒的に安価で素晴らしい機械的性能(強さ,硬さなど)を有している等の長所により,近代社会では,人間が必要とする機械設備,自動車,建築構造物などに数多く利用されていることは衆知である.その歴史は紀元前3000年前頃のメソポタミヤ文明までさかのぼり現代まで約5000年間,人間社会で使用されている.これからも貢献し続けると思われる.
しかしながら,鉄鋼材料の欠点の一つとして,大気・水中で使用された場合,その表面に錆が発生し,長期的には機械的性能が著しく低下する.この欠点を解決するために,鉄鋼材料に発生する錆を防ぐためのいろいろな技術が開発・実用されている.
以下,その技術の一つである表面処理の中の溶射法を用いた防食技術の基礎知識を紹介する.できるだけ平易な解説を心掛けるが,難しい点があれば“溶射”だけに“容赦”していただきたい.
2. 溶射とは (溶射技術のイロハ)
イ)溶射の原理
溶射(Thermal Spraying)とは「燃焼又は電気エネルギーを用いて溶射材料を加熱し,溶融又はそれに近い状態にした粒子を素地に吹き付けて皮膜を成膜すること」とJIS H 8200溶射用語で定義している.図1.に溶射の原理を示す.
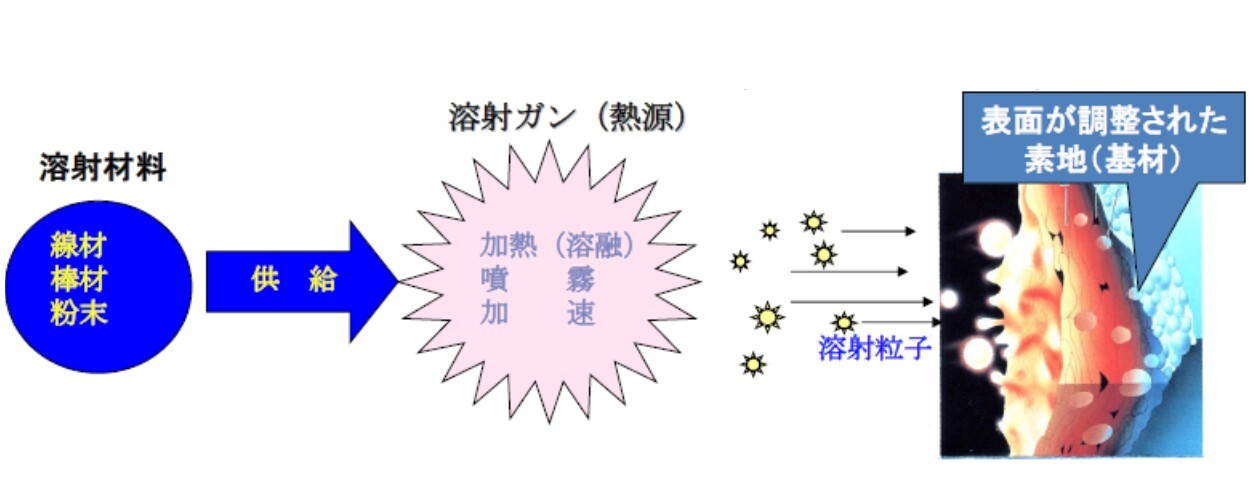
図1 溶射の原理(イメージ図)
溶射材料(2.ハ)項で詳述)を溶射ガン(熱源)に供給して,加熱・溶融し,噴霧ガスにより溶融粒子を形成・加速し,予め表面を調整(主にブラスト処理)した素地(基材)に衝突させて積層成膜するものである.
ロ)溶射法(溶射プロセス)
図2.に示す溶射法が実用されている.
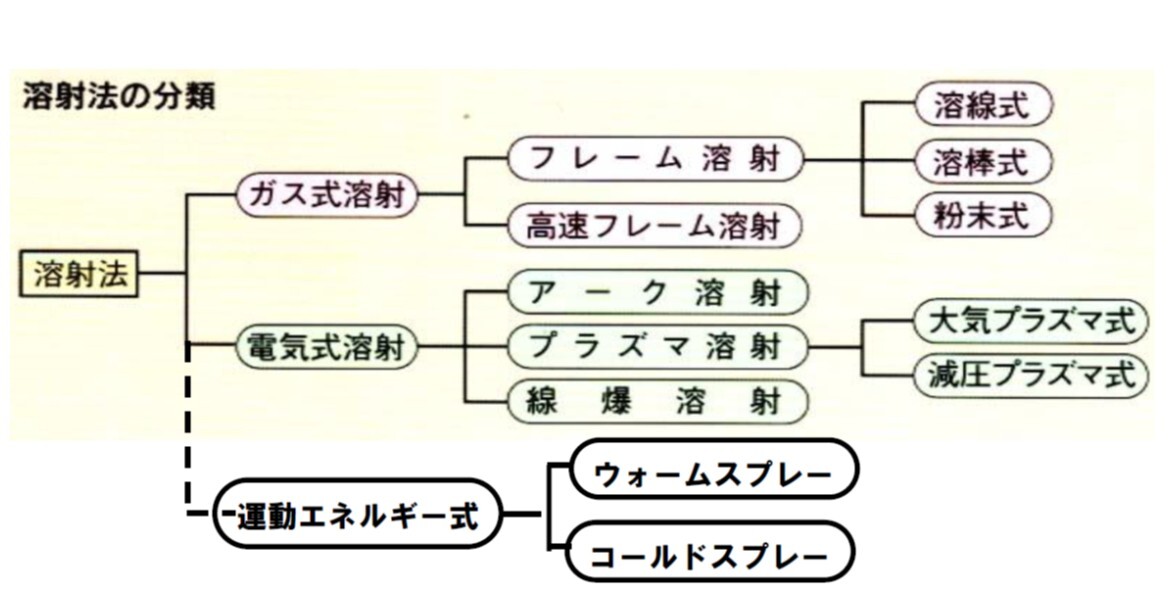
図2 溶射法の分類
ハ)溶射材料
図3.に溶射材料の形態,種類及び適用可能な溶射プロセスを示す.
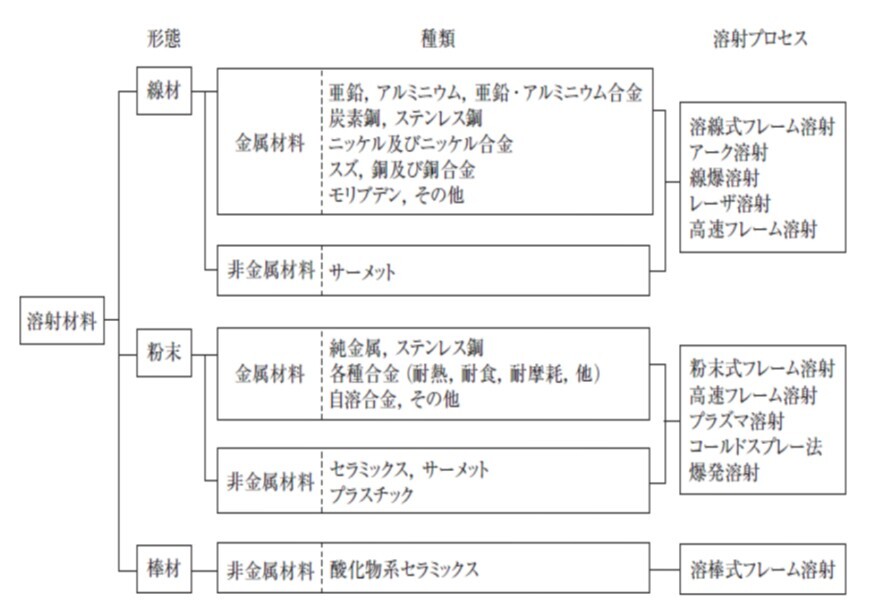
図3 溶射材料の形態,種類と使用される溶射プロセス4)
溶射材料の形態としては線材,粉末(スラリーを含む)及び棒材に分類される.種類としては金属(合金)材料,セラミック材料,サーメット(金属とセラミックの複合)材料及び樹脂材料がある.溶射材料として具備すべき条件は,融点を有し,蒸気圧・溶融時の粘性が低いなどが必要である.
3. 鉄鋼材料はなぜ錆びる?
イ)自然界の現象
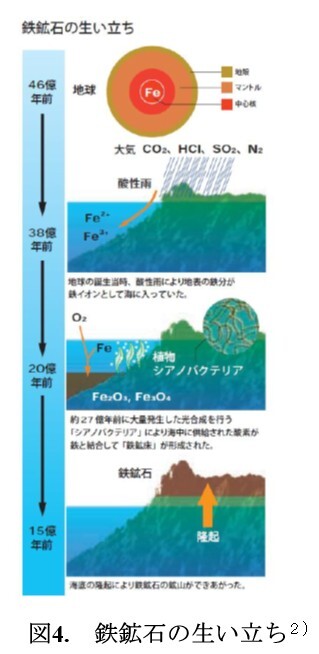
図4.に示す鉄鉱石の生い立ちから,鉄(Fe)の原料である鉄鉱石(主に,酸化鉄,Fe2O3など)は,太古の昔に存在した地表近くの鉄金属が自然と酸化されてできたものである(酸化反応).
2Fe + 3/2 O2 → Fe2O3 (1)
つまり,金属鉄は酸素(O2)と水(H2O)がある環境中では自然に酸化物にもどっていく. これが鉄の腐食(錆)である. 自然界ではFe よりも安定なFe2O3に自発的に変化する(化学反応).
自発的な化学反応が起こるのは,反応によりエネルギー的に安定な状態になるからである.
ロ)製鉄による鉄の製造
高炉では高温での化学反応によって,原料である鉄鉱石(酸化鉄)からコークス(C:炭素)により酸素を奪い, Feに変化させている(還元反応).
Fe2O3 + 3C →2Fe + 3CO (2)
この場合には大きなエネルギーを加えて,自発的には進まない反応を起こさせている.
高炉で創られる銑鉄はFe-C系の合金である.
ハ)鉄の湿式腐食モデル
磨いた鉄板表面に0.1mol 塩化ナトリウム水溶液にフェリシアン化カリウム[注1]を含むフェロキシル試薬または0.1mol 塩化ナトリウム水溶液にフェノールフタレイン[注2]を含むそれぞれの水溶液をスポイトで数滴たらし液滴を作り,液滴中の鉄板の変化を観察する.
その時の液滴内の変化は,滴下数分後には図5(a)に示すように液滴中心部の色が濃青色を呈するとともに,図5(b)に示すように液滴周辺部はピンク色を呈する様子が観察される.
[注1]フェリシアン化カリウム:鉄Fe2+イオンがあると反応して,濃青色に発色する化合物で,鉄イオンの存在の確認に用いられる.
[注2]フェノールフタレイン:酸性・中性では無色,アルカリ性では赤紫色(濃い桃色)に発色する色素.
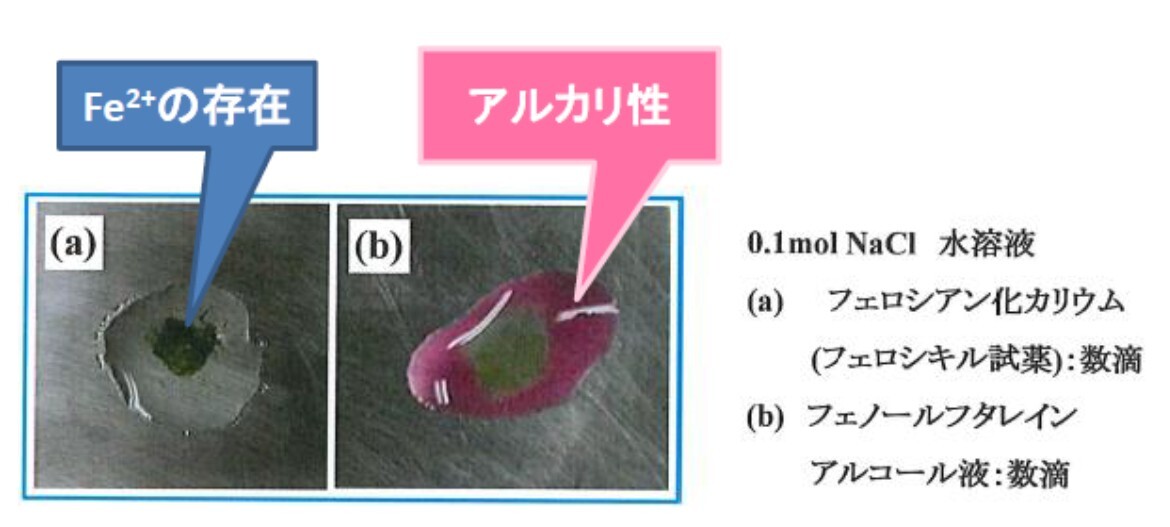
図5 液滴中の鉄板の変化4)
水滴内での鉄の腐食機構を図6.に示す.
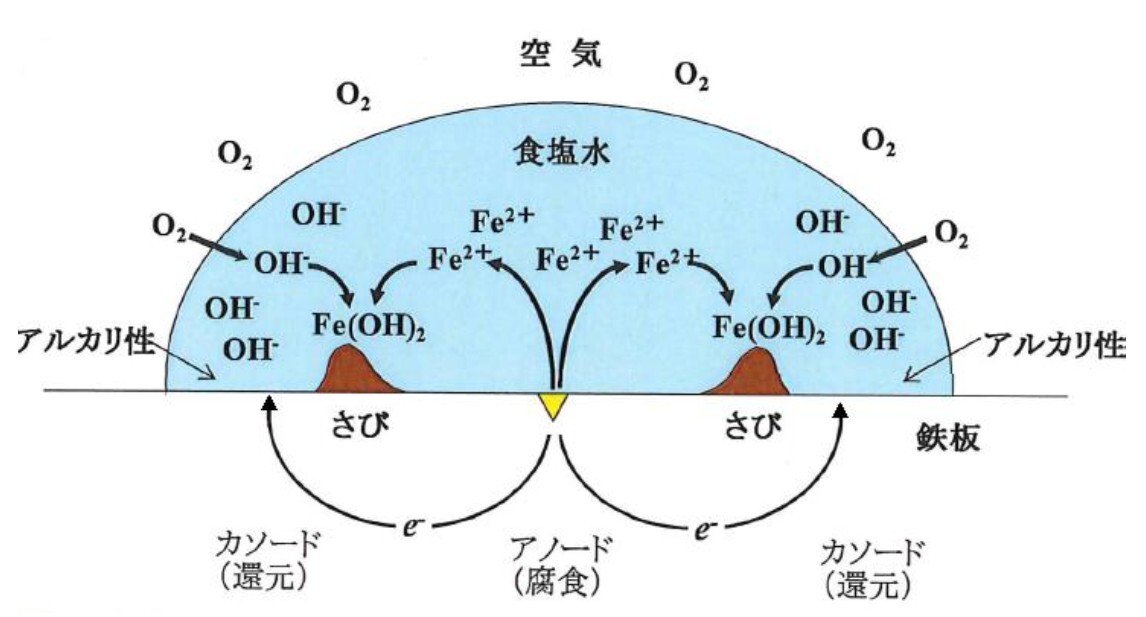
図6. 水滴内での鉄(Fe)の腐食機構4)
液滴中心の濃青色部では,次の反応が起っていると考えられる.
Fe → Fe2+ + 2e- (3)
この反応は電子を放出する反応で酸化反応といい,電気化学的にはアノード反応と呼ぶ.
周辺部のアルカリ性になった部分の反応は,電子が中心部から金属を通して動いてきて,次の反応が起こることによる.
1/2O2 + H2O + 2e- → 2OH- (4)
この反応は電子を受け取る反応で還元反応といい,電気化学的にはカソード反応と呼ばれる.
(3)と(4)の両式から腐食の全反応は以下の式で表される.
Fe + 1/2O2 + H2O → Fe2+ + 2OH- (5)
Fe + 1/2O2 + H2O → Fe(OH)2 (6)
(6)式右辺のFe2+は水酸化第一鉄 (Fe(OH)2)となり沈殿する.しかし,この物質はきわめて酸化されやすいため, 水中あるいは空気中の酸素により酸化され,最終的には酸化鉄(錆:水酸化鉄・オキシ水酸化鉄を含む)に変化する.
4. 防食溶射技術の紹介
イ)鉄の防食手法
図7.に示す鉄の電位-pH図において,中性水溶液(pH=7)中の鉄は,電位-0.440V(vs. SHE) であるA点にある.このまま放置すれば腐食域にあるから,赤錆を発生して腐食は継続的に進んでしまう.
鉄の腐食を防ぐためには,A点から安全な領域に状態を移動させる必要がある. そのために3つの方向がある.
① 電位を不活性域まで低電位(卑な方向)へ移動させる(犠牲防食).
② 電位を不働態域まで高電位(貴な方向)へ移動させる(アノード防食[注3]).
③ 環境のpHを増大させ,不働態に移動させる.
鉄鋼材料に対して,亜鉛(Zn), アルミニウム(Al),マグネシウム(Mg)及びそれらの合金類の溶射皮膜を施工する防食技術は,これらの皮膜金属のもつ低い電極電位により①を実現することにより腐食を防止しようとするもので,熱力学的原理にかなった有効な防食手段である.
実際の溶射施工においては,このような防食作用が最大限に発揮できるように,溶射作業工程や品質管理に留意する必要がある.
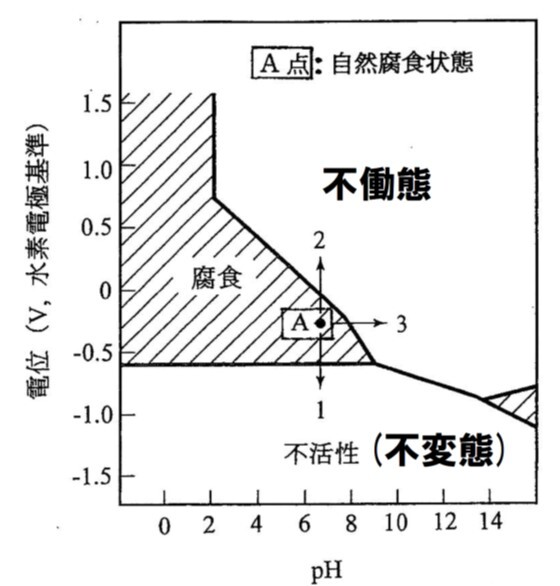
図7 鉄の電位-pH図と防食手法1)
[注3]アノード防食:鉄やステンレス鋼などいくつかの金属は,アノード分極によって不働態領域へ移行させれば効果的に防食できる.電位を自動的に不働態領域に保持するにはポテンショスタットが用いられる.アノード防食法の応用はとくに硫酸を扱う場合に有効である.
ロ)防食溶射の位置づけ
図8.に代表的な防食方法を示す.防食方法の皮膜防食で金属皮膜の一つとして溶射技術(防食溶射)がある.
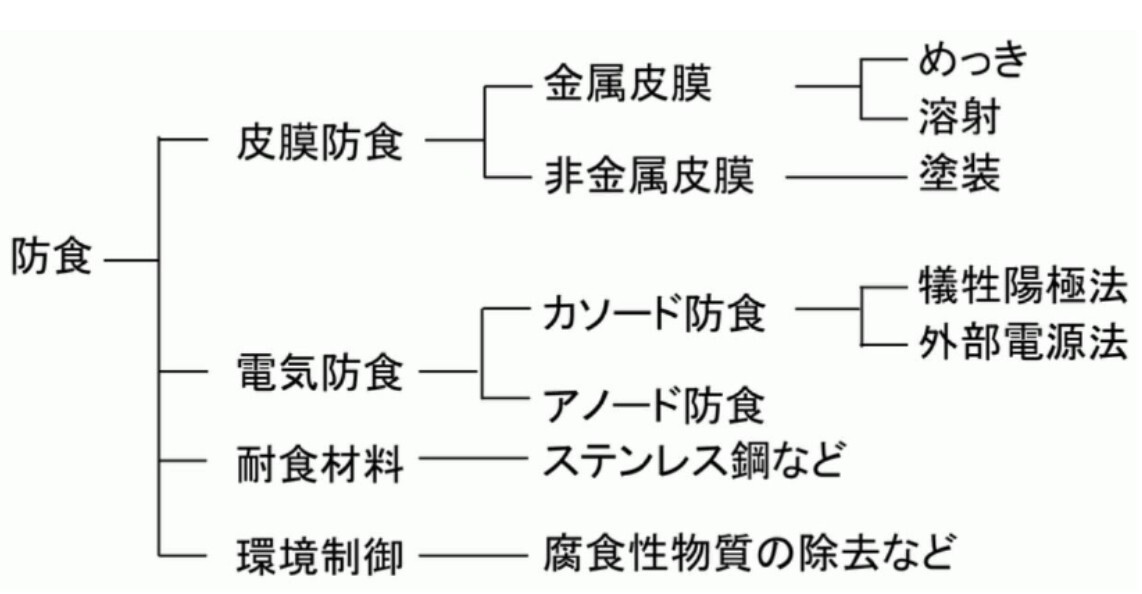
図8 代表的な防食方法3)
ハ)防食溶射の種類・材料・溶射法
図9.に防食溶射の種類,材料,溶射方法,防食のメカニズム及び応用例を示す.
構造物等の素材(基材)金属が腐食されることを防止することを目的に施工される溶射法が,「防食溶射」である.その腐食の種類・腐食原因により,主に3つの溶射法に分類される.
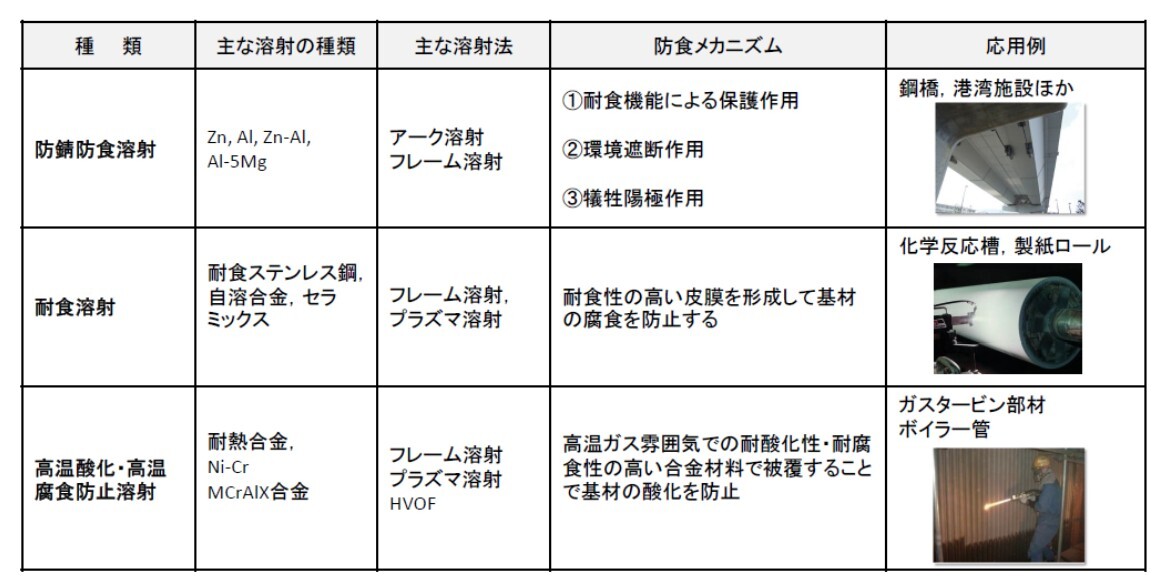
図9 防食溶射の概要4)
6. おわりに
防食溶射技術はReduce(リデュース:耐久性の高い製品の提供や製品寿命延長)やReuse(リユース:溶射の再施工で使用済製品やその部品等を繰り返し使用すること)に繋がる技術として工業的に利用され,鉄鋼材料の腐食対策費(年間約4兆円)の一部の削減に貢献している.
<参考文献>
1)上野和夫他:溶射技術入門(四訂版)一般社団法人日本溶射学会 2020
2)日本製鉄株式会社ホームページ モノづくりの原点 科学の世界VOL.15:V15.pdf
3)福﨑 昌宏:防食の分類とは:金属材料基礎講座(その75):モノつくりドットコム
4)日本溶射学会 溶射管理士資格認定講習 防食溶射テキスト

【執筆者】
坂田一則 技術士・労働安全コンサルタント事務所
所長 坂田一則
技術士(金属・総合技術監理部門)
労働安全コンサルタント(機械)
博士(工学)九州大学
(日本技術士会九州本部/北九州)
【専門事項】
① 中小企業の技術経営・研究開発(主に表面技術)・安全活動支援,
② ビジネスマッチング支援,
③ 大学・高専の学生のインターンシップと中小企業の受入れに関するコーディネート,
④ 公的機関の補助金等の申請支援等の中小企業勤務経験を活かした中小企業目線での支援を“一味同心”に務めること心掛けている.
※本記事のご利用にあたって
本記事の内容は執筆者個人の見解に基づくものであり、日本技術士会の公式見解ではありません。また、記事の内容は執筆時点の情報に基づいています。ご利用者様自身の判断と責任において、ご活用頂くようお願いいたします。











